文献速览 | 铜绿假单胞菌铁获取新机制T6SS效应蛋白研究
- 看不见的线
- 2705
- 2025-03-28 08:23:18
- 原创
文章题目:A Pseudomonas T6SS effector recruits PQS-containing outer membrane vesicles for iron acquisition
文章链接:https://doi.org/10.1038/ncomms14888
发表时间:2017.03
期刊:Nature communications
影响因子:14.7

研究概述
这篇论文研究了铜绿假单胞菌(Pseudomonas aeruginosa)的铁获取机制。研究发现,该菌种存在一种新的铁获取途径,其中一个名为PA2374(现命名为TseF)的基因与已知的铁获取系统协同作用。TseF蛋白通过VI型分泌系统(H3-T6SS)分泌,并与细胞间信号分子PQS结合,随后被纳入外膜囊泡(OMVs)中。通过与Fe(III)-pyochelin受体FptA和孔蛋白OprF相互作用,TseF蛋白能够促进OMVs中结合的铁被细菌细胞利用。研究结果揭示了VI型分泌系统、细胞间信号传递与经典铁载体受体在铜绿假单胞菌铁获取过程中的联系。
研究背景
铁是细菌生长和毒力的必需元素,但宿主可以通过铁螯合蛋白限制细菌的铁摄取,从而抵御病原体感染。铜绿假单胞菌(Pseudomonas aeruginosa)已知依赖三种铁获取系统(pyoverdine、pyochelin、Feo系统),但新发现的三突变体株(ΔpvdA/ΔpchE/ΔfeoB)仍能在缺铁条件下生长,这表明在铜绿假单胞菌中可能还存在其它未知的铁吸收途径。
研究结果
01 H3-T6SS邻近基因在铁获取中起重要作用
为研究是否存在其他铁获取机制,研究人员基于转座子突变筛选构建了三重突变体PAΔ3Fe(缺失pyoverdin、pyochelin和FeoB系统)。结果发现H3-T6SS邻近基因PA2374(命名为TseF)与已知铁获取系统协同作用,可促进细菌在缺铁培养基中的生长。tseF缺失突变体在缺铁条件下无法生长,但回补pvdA或tseF可恢复生长,且pvdA效果更强,表明PvdA系统在铁吸收中更高效。
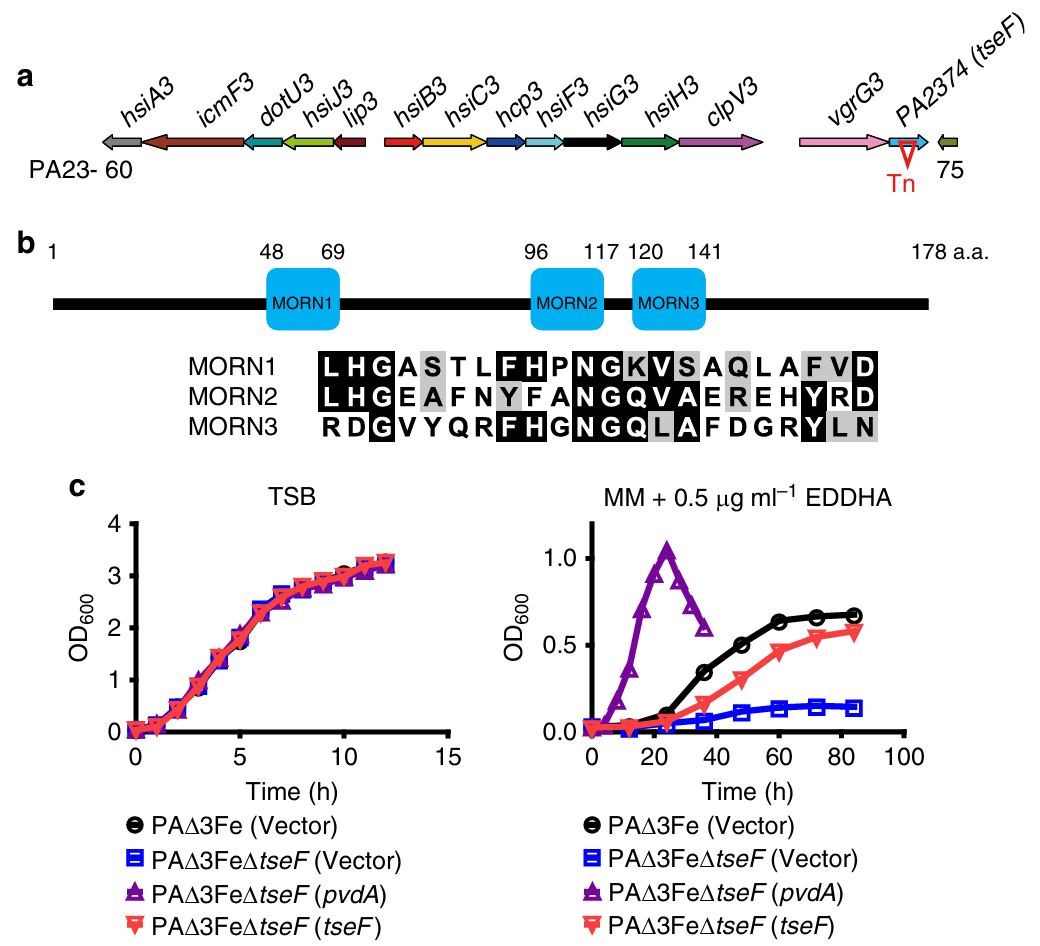
图 1 (a) H3-T6SS及其邻近基因的组成结构;(b) TseF的结构域;(c) 突变体在缺铁培养基中的生长曲线。相关菌株在TSB或含有EDDHA(0.5 mg ml 1)的琥珀酸MM中培养。通过测量OD600来监测细胞生长。
02 TseF是H3-T6SS的底物
图2(a)实验发现,TseF在野生型细菌的培养上清液中可被检测到,在缺失H3-T6SS关键组分(如ClpV3或HsiB3-C3)的突变体中,其分泌显著减少但未完全消失。Hcp3的分泌也表现出类似模式。图2(b)实验显示,TseF能与VgrG3和VgrG1b结合,但不与VgrG1a结合,且不与无关蛋白PA0533相互作用。这些结果说明TseF可能是H3-T6SS的底物,并通过与VgrG蛋白的选择性结合实现分泌。TseF在H3-T6SS突变体中的残留分泌可能与其他T6SS系统(如H1-和H2-T6SS)的识别有关。
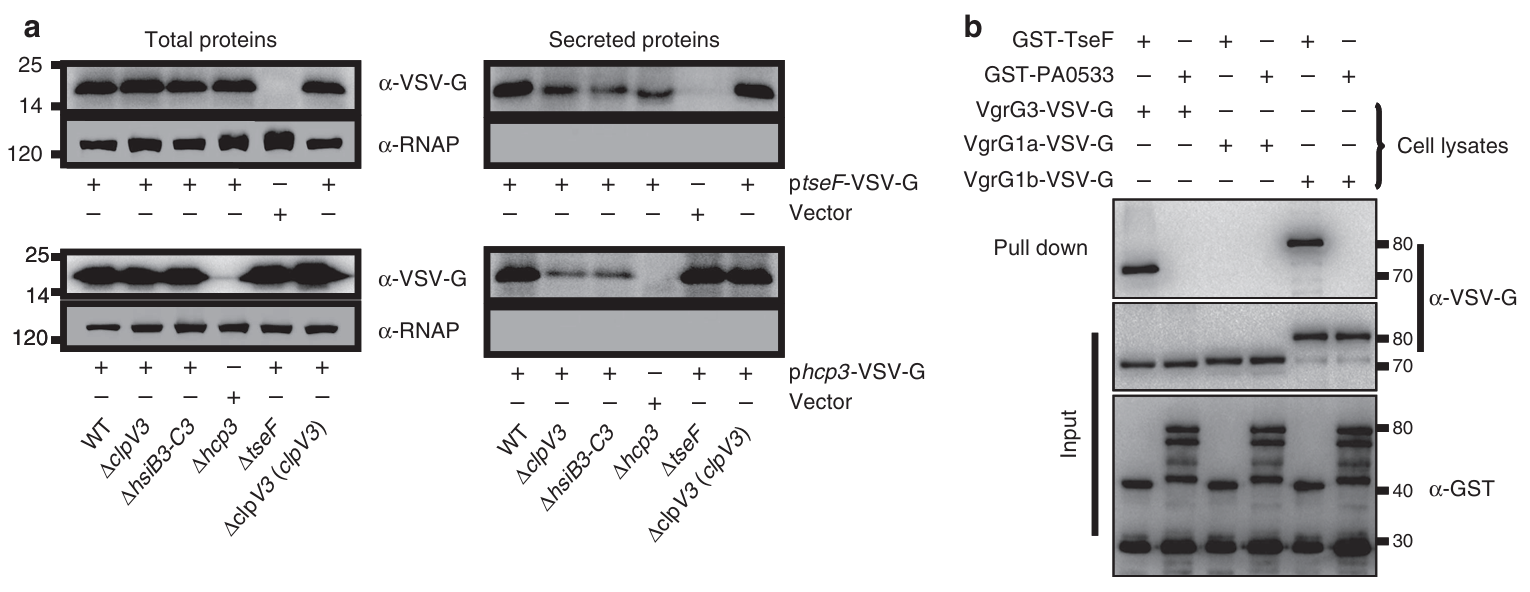
图2 (a) 培养上清液中的总蛋白和分泌蛋白变化;(b) TseF与VgrG3、VgrG1b的相互作用。
03 TseF与PQS相互作用
TseF在缺铁条件下对细菌生长至关重要,但它并不直接与铁离子结合,而是通过与PQS相互作用,参与铁吸收。实验结果显示,TseF与铜绿假单胞菌培养上清液中的PQS结合,导致PQS的丰度显著降低。PQS是一种铁螯合分子,其生物合成依赖于las和rhl群体感应系统。通过LC-MS和结合实验,证实TseF与PQS特异性结合,且结合亲和力在铁离子存在时增强。此外,TseF的表达恢复了PAΔ3FeΔtseF突变体在PQS-Fe³⁺作为唯一铁源时的生长能力,表明TseF通过结合PQS-Fe³⁺复合物参与铁的吸收。因此TseF通过与PQS的相互作用在铁获取中起关键作用。
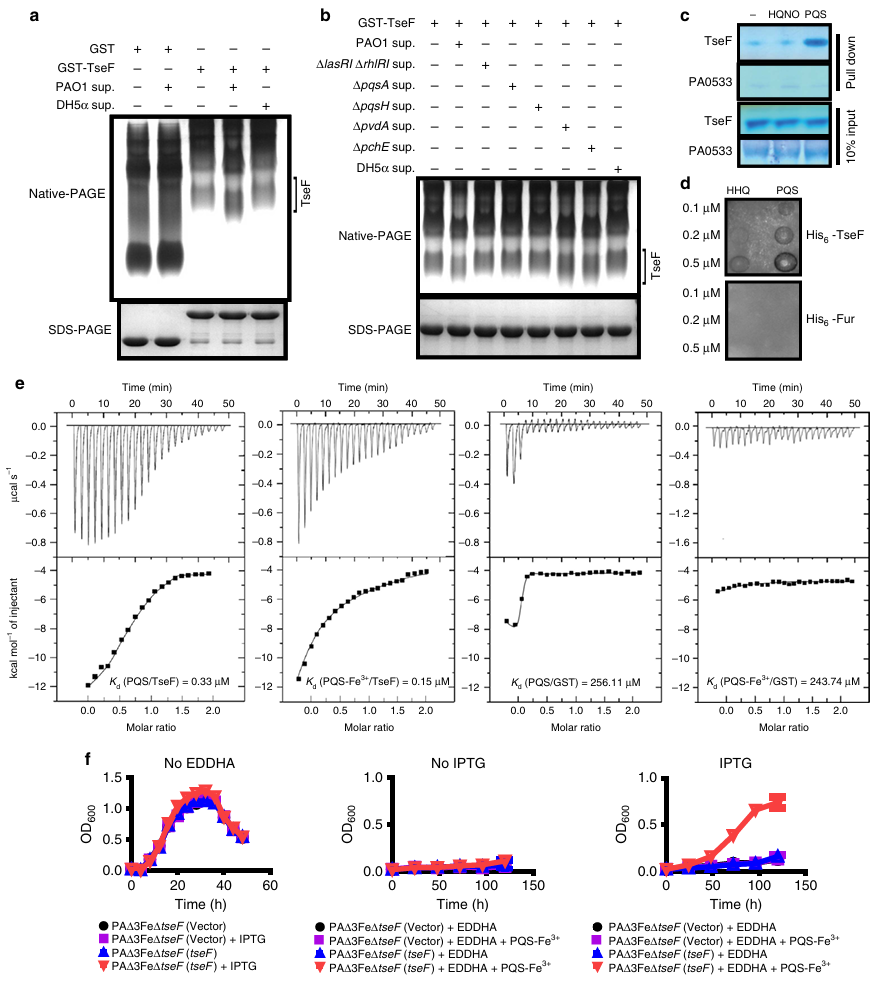
图 3 (a) TseF与铜绿假单胞菌培养上清液的相互作用;(b) 喹诺酮信号对TseF迁移率的影响;(c) TseF能与固定的PQS结合;(d) His6-TseF能与膜上固定的PQS结合;(e) Fe³⁺增强了PQS与TseF的结合;(f) PQS-Fe³⁺的供铁依赖TseF。
04 FptA/OprF是TseF介导的铁获取所必需的
TseF、PQS和Fe³⁺之间的高亲和力结合表明它们形成复合物。为研究铁如何通过该复合物进入细胞,研究人员假设TseF通过与细菌表面的受体蛋白结合来传递铁离子。基于亲和层析实验、质谱分析及验证分析,作者发现TseF与OprF(孔蛋白)和FptA(Fe(III)-pyochelin受体)相互作用。为确定两者在TseF介导的铁吸收中的作用,研究人员构建了PAΔ3FeΔtseFΔfptAΔoprF突变体。该突变体在富铁培养基中生长正常,但无法利用PQS-Fe³⁺作为唯一铁源生长。只有当TseF与FptA或OprF同时表达时,细菌才能利用PQS-Fe³⁺维持生长。这些结果表明,TseF在铁获取中的作用是通过将PQS-Fe³⁺桥接到受体FptA或OprF上来实现的。
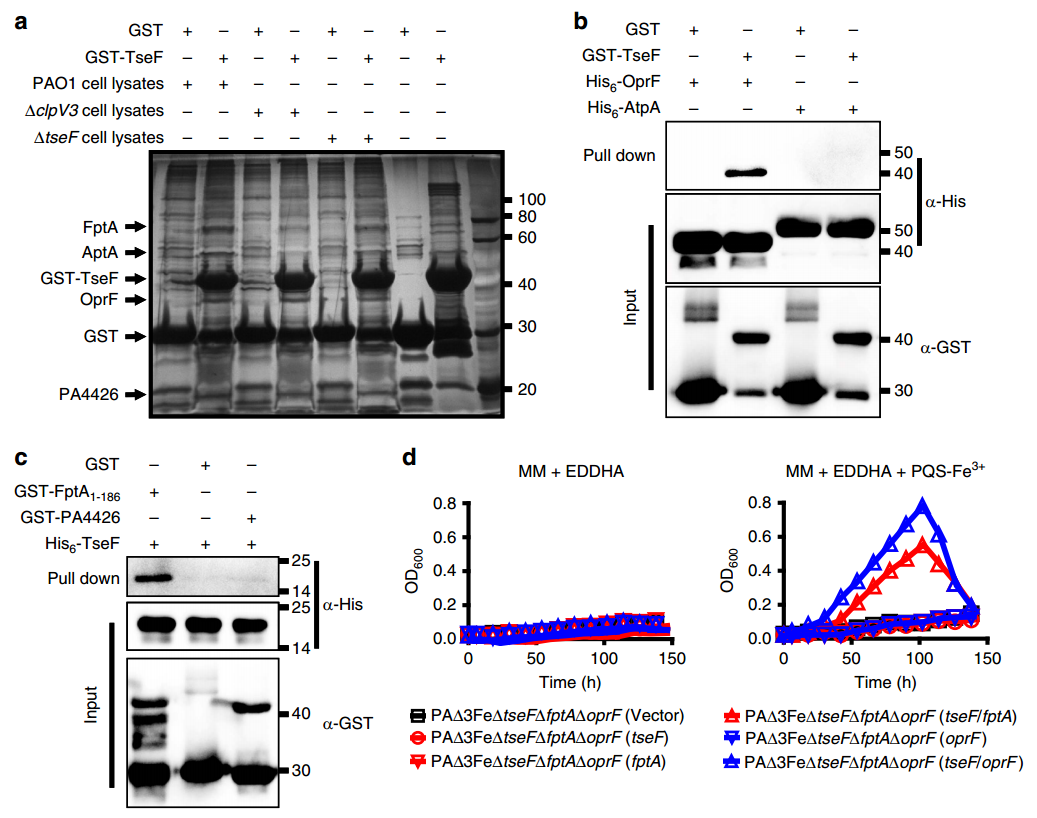
图 4 (a) 鉴定OprF和FptA为TseF的结合伴侣;(b) TseF与OprF的直接相互作用;(c) TseF与FptA的直接相互作用;(d) OprF和FptA在PQS-Fe³⁺供铁中的作用。
05 TseF被整合到OMV中以获取铁
PQS通常包裹在外膜囊泡(OMVs)中,参与多种信号传递事件。研究发现,TseF通过与PQS结合的OMVs参与铁的吸收。实验显示,TseF以PQS依赖的方式与OMVs结合,而缺失TseF或PQS合成基因的突变体无法将TseF整合到OMVs中。野生型OMVs能够促进PAΔ3FeΔtseF在缺铁条件下的生长,而缺失TseF的OMVs则无此功能。进一步实验表明,TseF与FptA/OprF受体在同一铁吸收途径中发挥作用,缺失这些受体的突变体无法利用OMVs供铁。此外,H3-T6SS系统在TseF介导的铁吸收中起关键作用,缺失H3-T6SS核心组分(如ClpV3)或TseF的突变体在宿主中竞争能力下降,表明TseF介导的铁吸收对铜绿假单胞菌的毒力至关重要。
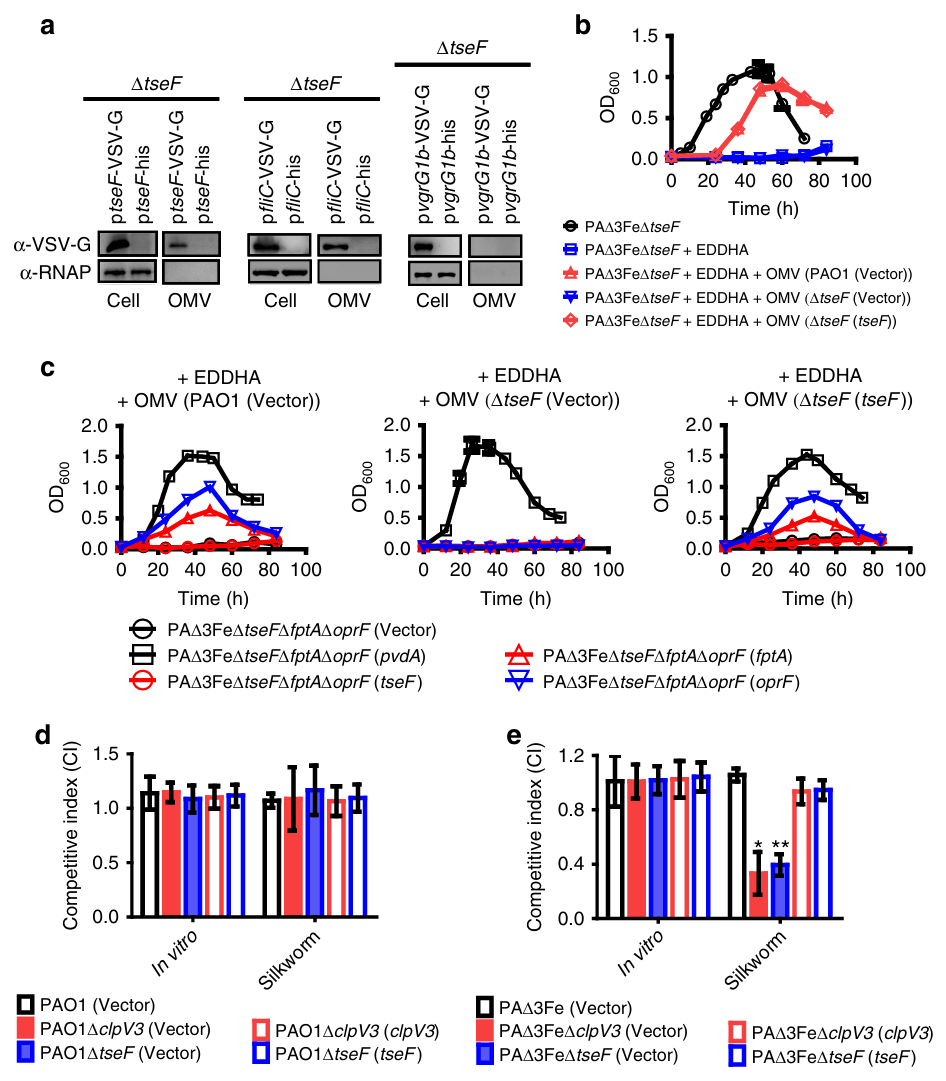
图 5 (a) TseF整合到OMV复合物中;(b) TseF是OMVs供铁的必要条件;(c) OMVs供铁需要OprF或FptA;(d, e) TseF铁吸收系统在宿主中的重要性。
总结
本文揭示了一种新型的铁摄取机制,涉及T6SS效应蛋白TseF、PQS信号分子和OMVs的相互作用。TseF通过与PQS结合,将OMVs中的铁转运到细菌细胞内,从而在铁缺乏条件下维持细菌的生长和毒力。这一发现揭示了铜绿假单胞菌铁摄取的新机制,扩充了pyoverdin、pyochelin和FeoB铁载体系统缺失情况下铁摄取的认知,为理解细菌如何通过分泌系统和信号分子适应宿主环境提供了新的视角。
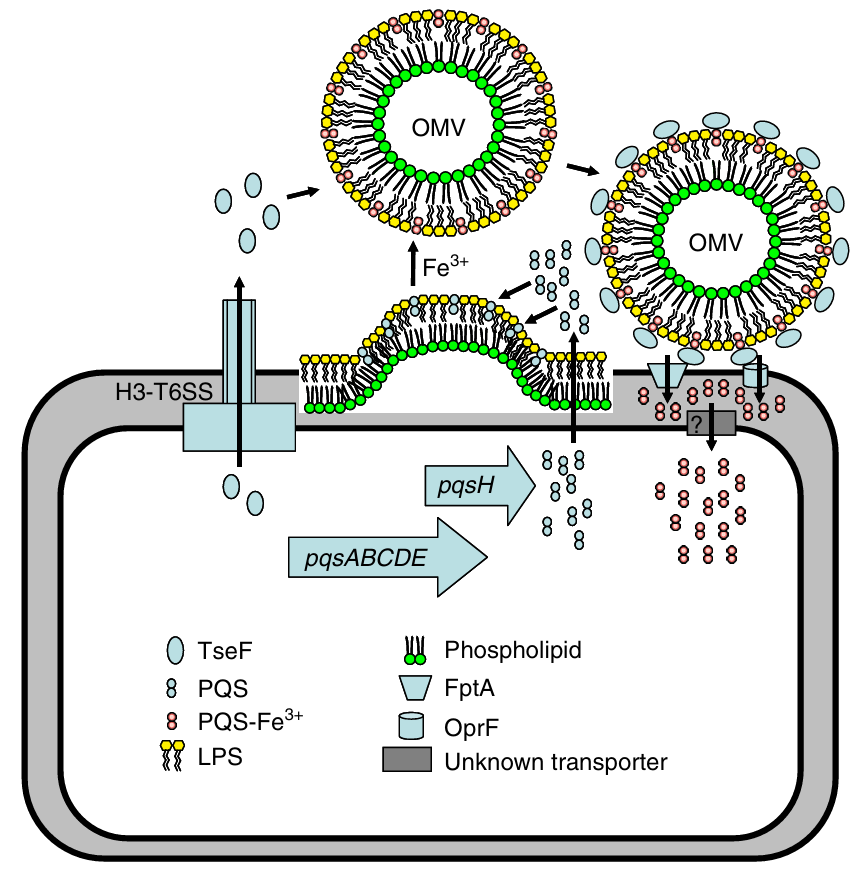
图 6 TseF介导铁获取与OMV复合物结合的模型图
(TseF由H3-T6SS分泌,然后与OMV复合物外侧的PQS-Fe³⁺结合;细胞表面受体FptA或OprF对TseF的识别途径暂未确认)。
参考文献
Lin J, Zhang W, Cheng J, Yang X, Zhu K, Wang Y, Wei G, Qian PY, Luo ZQ, Shen X. A Pseudomonas T6SS effector recruits PQS-containing outer membrane vesicles for iron acquisition. Nature Communications, 2017, 8(1): 14888.
课程推荐
-
点赞 (0人)
- 收藏 (0人)



